कोविडसाठी Pfizer च्या mRNA लसीने उपचारात्मक लक्ष्य म्हणून रिबोन्यूक्लिक अॅसिड (RNA) वापरण्याची आवड पुन्हा जागृत केली आहे.तथापि, लहान रेणूंसह आरएनए लक्ष्य करणे अत्यंत आव्हानात्मक आहे.
RNA मध्ये फक्त चार बिल्डिंग ब्लॉक्स असतात: एडिनाइन (A), सायटोसिन (C), ग्वानिन (G), आणि uracil (U) जे DNA मध्ये आढळणाऱ्या थायमिन (T) ची जागा घेतात.हे औषध निवडण्याला जवळजवळ दुर्गम अडथळा बनवते.याउलट, 22 नैसर्गिक अमीनो ऍसिड आहेत जे प्रथिने बनवतात, जे स्पष्ट करते की बहुतेक प्रथिने-लक्ष्यीकरण औषधांची निवड तुलनेने चांगली का असते.
आरएनएची रचना आणि कार्य
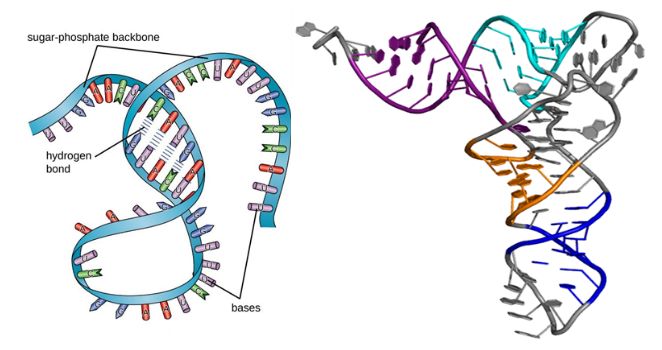
प्रथिनांप्रमाणेच, RNA रेणूंची दुय्यम आणि तृतीयक रचना असते, खालील आकृतीत दर्शविल्याप्रमाणे.जरी ते सिंगल-चेन मॅक्रोमोलेक्यूल्स असले तरी, जेव्हा बेस पेअरिंगमुळे फुगे, लूप आणि हेलिकेस होतात तेव्हा त्यांची दुय्यम रचना आकार घेते.त्यानंतर, त्रिमितीय फोल्डिंग RNA च्या तृतीयक संरचनेकडे नेतो, जी त्याच्या स्थिरता आणि कार्यासाठी आवश्यक आहे.
आकृती 1. आरएनएची रचना
आरएनएचे तीन प्रकार आहेत:
- मेसेंजर आरएनए (mRNA)डीएनए मधून अनुवांशिक माहितीचे प्रतिलेखन करते आणि मूळ क्रम म्हणून राइबोसोमवर हस्तांतरित केले जाते;l
- रिबोसोमल आरएनए (आरआरएनए)राइबोसोम नावाच्या प्रथिने-संश्लेषण करणाऱ्या ऑर्गेनेल्सचा एक भाग आहे, जो साइटोप्लाझममध्ये निर्यात केला जातो आणि mRNA मधील माहिती प्रथिनांमध्ये अनुवादित करण्यात मदत करतो;
- आरएनए (tRNA) हस्तांतरित कराmRNA आणि प्रथिने बनवणाऱ्या अमिनो आम्ल साखळीतील दुवा आहे.
RNA ला उपचारात्मक लक्ष्य म्हणून लक्ष्य करणे खूप आकर्षक आहे.असे आढळून आले आहे की आपल्या जीनोमपैकी फक्त 1.5% अंततः प्रथिनांमध्ये अनुवादित केले जाते, तर 70%-90% RNA मध्ये लिप्यंतरण केले जाते.आरएनए रेणू सर्व सजीवांसाठी सर्वात महत्वाचे आहेत.फ्रान्सिस क्रिकच्या "केंद्रीय मतप्रणाली" नुसार, आरएनएची सर्वात महत्वाची भूमिका म्हणजे डीएनए मधून प्रथिनांमध्ये अनुवांशिक माहितीचे भाषांतर करणे.याशिवाय, आरएनए रेणूंची इतर कार्ये देखील आहेत, यासह:
- प्रथिने संश्लेषणात अडॅप्टर रेणू म्हणून काम करणे;l
- डीएनए आणि राइबोसोम दरम्यान संदेशवाहक म्हणून काम करणे;l
- ते सर्व जिवंत पेशींमध्ये अनुवांशिक माहितीचे वाहक आहेत;l
- नवीन प्रथिनांचे संश्लेषण करण्यासाठी आवश्यक असलेल्या योग्य अमीनो ऍसिडच्या राइबोसोमल निवडीला प्रोत्साहन देणेvivo मध्ये.
प्रतिजैविक
1940 च्या दशकाच्या सुरुवातीस शोधूनही, अनेक प्रतिजैविकांच्या कृतीची यंत्रणा 1980 च्या उत्तरार्धापर्यंत स्पष्ट केली गेली नव्हती.असे आढळून आले आहे की प्रतिजैविकांचा एक मोठा भाग बॅक्टेरियाच्या राइबोसोमला योग्य प्रथिने बनवण्यापासून रोखण्यासाठी त्यांना बांधून कार्य करतो, ज्यामुळे जीवाणू नष्ट होतात.
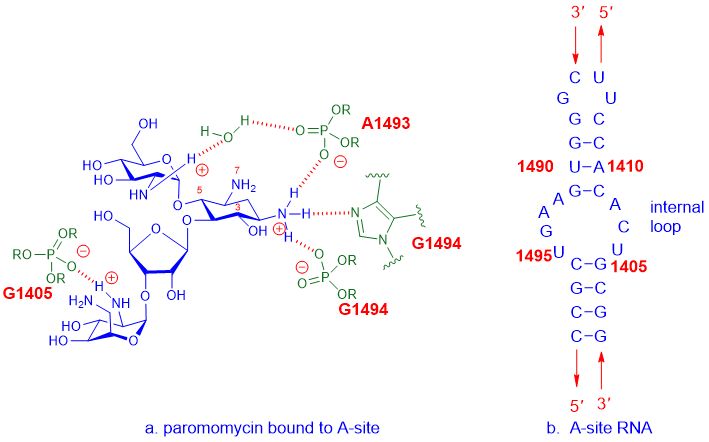
उदाहरणार्थ, अमिनोग्लायकोसाइड अँटीबायोटिक्स 16S rRNA च्या A-साइटला बांधतात, जो 30S राइबोसोम सब्यूनिटचा भाग आहे आणि नंतर प्रथिने संश्लेषणात व्यत्यय आणून जिवाणूंच्या वाढीस व्यत्यय आणतो, शेवटी सेलचा मृत्यू होतो.ए-साइट एमिनोएसिल साइटचा संदर्भ देते, ज्याला टीआरएनए स्वीकारणारी साइट देखील म्हणतात.एमिनोग्लायकोसाइड औषधांमधील तपशीलवार संवाद, जसे कीपॅरोमोमायसिन, आणि ची ए-साइटई कोलाय्आरएनए खाली दर्शविले आहे.
आकृती 2. पॅरोमोमायसिन आणि ए-साइट यांच्यातील परस्परसंवादई कोलाय्आरएनए
दुर्दैवाने, एमिनोग्लायकोसाइड औषधांसह अनेक ए-साइट इनहिबिटरमध्ये नेफ्रोटॉक्सिसिटी, डोस-आश्रित आणि विशिष्ट अपरिवर्तनीय ओटोटॉक्सिसिटी यासारख्या सुरक्षा समस्या आहेत.आरएनए लहान रेणू ओळखण्यासाठी एमिनोग्लायकोसाइड औषधांमध्ये निवडकतेच्या कमतरतेमुळे हे विषारी पदार्थ आहेत.
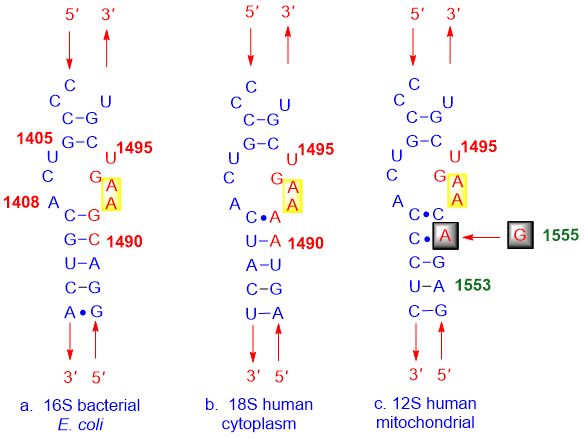
खालील आकृतीत दाखवल्याप्रमाणे: (a) जीवाणूंची रचना, (b) मानवी पेशीचा पडदा आणि (c) मानवी माइटोकॉन्ड्रियल ए-साइट खूप समान आहेत, ज्यामुळे ए-साइट इनहिबिटर या सर्वांशी बांधील होतात.
आकृती 3. नॉन-सिलेक्टिव्ह ए-साइट इनहिबिटर बंधनकारक
टेट्रासाइक्लिन अँटीबायोटिक्स देखील आरआरएनएच्या ए-साइटला प्रतिबंधित करतात.Mg सह कॉम्प्लेक्स असलेल्या 30S सबयुनिटवर उलट्या रीतीने हेलिकल प्रदेश (H34) ला जोडून ते निवडकपणे जिवाणू प्रोटीन संश्लेषण रोखतात.2+.
दुसरीकडे, मॅक्रोलाइड अँटीबायोटिक्स नवजात पेप्टाइड्स (NPET) साठी बॅक्टेरियाच्या राइबोसोम बोगद्याच्या बाहेर पडण्याच्या साइट (ई-साइट) जवळ बांधतात आणि अंशतः अवरोधित करतात, ज्यामुळे बॅक्टेरियाच्या प्रथिने संश्लेषणास प्रतिबंध होतो.शेवटी, oxazolidinone प्रतिजैविक जसेलाइनझोलिड(Zyvox) 23S rRNA न्यूक्लियोटाइड्सने वेढलेल्या जिवाणू 50S राइबोसोमल सब्यूनिटमध्ये खोल फाटावर बांधला जातो.
अँटिसेन्स ऑलिगोन्यूक्लियोटाइड्स (ASO)
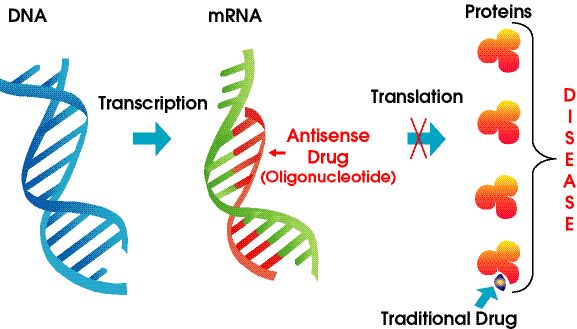
अँटीसेन्स औषधे ही रासायनिक-सुधारित न्यूक्लिक अॅसिड पॉलिमर आहेत जी आरएनएला लक्ष्य करतात.लक्ष्य mRNA ला बांधण्यासाठी ते वॉटसन-क्रिक बेस पेअरिंगवर अवलंबून असतात, परिणामी जीन सायलेन्सिंग, स्टेरिक ब्लॉकेड किंवा स्प्लिसिंग फेरफार होते.एएसओ सेल न्यूक्लियसमधील प्री-आरएनए आणि सायटोप्लाझममधील परिपक्व एमआरएनएशी संवाद साधू शकतात.ते exons, introns आणि untranslated Region (UTR) ला लक्ष्य करू शकतात.आजपर्यंत, एक डझनहून अधिक ASO औषधांना FDA ने मान्यता दिली आहे.
आकृती 4. अँटिसेन्स तंत्रज्ञान
RNA ला लक्ष्य करणारी लहान रेणू औषधे
2015 मध्ये, नोव्हार्टिसने नोंदवले की त्यांनी ब्रॅनप्लाम नावाचा SMN2 स्प्लिसिंग रेग्युलेटर शोधला आहे, जो U1-pre-mRNA चा संबंध वाढवतो आणि SMA उंदरांना वाचवतो.
दुसरीकडे, PTC/Roche's Risdiplam (Evrysdi) ला 2020 मध्ये FDA ने SMA च्या उपचारासाठी मान्यता दिली होती.ब्रॅनपलाम प्रमाणे, रिसडिप्लाम देखील कार्यशील SMN प्रथिने तयार करण्यासाठी संबंधित SMN2 जनुकांच्या विभाजनाचे नियमन करून कार्य करते.
आरएनए डिग्रेडर्स
RBM म्हणजे RNA-बाइंडिंग मोटिफ प्रोटीन.मूलत:, इंडोल सल्फोनामाइड एक आण्विक चिकट आहे.हे निवडकपणे RBM39 ला CRL4-DCAF15 E3 ubiquitin ligase मध्ये भरती करते, RBM39 पॉलीयुबिक्विटीनेशन आणि प्रोटीन डिग्रेडेशनला प्रोत्साहन देते.RBM39 चे अनुवांशिक घट किंवा सल्फोनामाइड-मध्यस्थ ऱ्हास लक्षणीय जीनोम-व्यापी स्प्लिसिंग विकृतींना प्रेरित करते, ज्यामुळे शेवटी सेल मृत्यू होतो.
RNA-PROTACs RNA-बाइंडिंग प्रोटीन (RBPs) कमी करण्यासाठी विकसित केले जातात.PROTAC E3 ligase ligand ला RNA ligand ला जोडण्यासाठी लिंकर वापरते, जे RNA आणि RBPs ला जोडते.RBP मध्ये विशिष्ट ऑलिगोन्यूक्लियोटाइड अनुक्रमांना बांधून ठेवू शकणारे स्ट्रक्चरल डोमेन असल्यामुळे, RNA-PROTAC आवडीच्या प्रोटीनसाठी (POI) लिगँड म्हणून ऑलिगोन्यूक्लियोटाइड अनुक्रम वापरते.अंतिम परिणाम म्हणजे RBPs चे ऱ्हास.
अलीकडेच, स्क्रिप्स इन्स्टिट्यूट ऑफ ओशनोग्राफीचे प्रोफेसर मॅथ्यू डिस्ने यांनी आरएनएचा शोध लावला.ribonuclease-लक्ष्यीकरण chimeras (RiboTACs).RiboTAC हा एक हेटरोफंक्शनल रेणू आहे जो RNase L ligand आणि RNA ligand ला लिंकरने जोडतो.हे विशिष्ट RNA लक्ष्यांमध्ये अंतर्जात RNase L ची भरती करू शकते आणि नंतर सेल्युलर न्यूक्लिक अॅसिड ब्रेकडाउन मेकॅनिझम (RNase L) वापरून RNA यशस्वीपणे काढून टाकू शकते.
लहान रेणू आणि आरएनए लक्ष्यांमधील परस्परसंवादाबद्दल संशोधक अधिक जाणून घेत असताना, भविष्यात ही पद्धत वापरणारी आणखी औषधे उदयास येतील.
पोस्ट वेळ: ऑगस्ट-02-2023